L’Osmose
Introduction
L’osmose est un phénomène physico-chimique fondamental qui intervient constamment en cuisine — souvent sans que nous en ayons conscience. Elle gouverne la manière dont l’eau circule dans les aliments, influence leur texture, modifie leur goût et conditionne l’efficacité de pratiques comme le salage, le dégorgement ou le confisage.
Comprendre l’osmose, c’est comprendre pourquoi un légume dégorge avec du sel, pourquoi une marinade pénètre plus ou moins profondément, ou pourquoi du saumon gravlax change complètement de texture.
C’est aussi poser les bases nécessaires pour comprendre la diffusion et l’activité de l’eau (Aw).
1. Définition
Définition Générale
L’osmose, c’est le mouvement de l’eau à travers une membrane qui laisse passer l’eau mais pas les solutés dissout dans l’eau (comme le sel ou le sucre). Elle se produit pour équilibrer les concentrations en soluté entre deux milieux (de chaque côté de la membrane).
En bref, l’eau se déplace vers la zone la plus concentrée en soluté (plus salée / plus sucrée) jusqu’à ce que les concentrations s’équilibre à nouveau.
Définition scientifique
En sciences, l’Osmose est définie comme :
Le passage spontané d’un solvant, en cuisine généralement des molécules d’eau, à travers une membrane semi-perméable, du milieu le moins concentré en solutés vers le milieu le plus concentré, jusqu’à équilibrer les pressions osmotiques (qu’on pourrait qualifier vulgairement de « force qui attire/retient l’eau »).
- La membrane semi-perméable est une barrière qui laisse passer l’eau mais pas certains solutés. En cuisine, ce sont principalement :
- Les membranes cellulaires
- Les parois des fibres musculaires
- À l’échelle technique, des membranes industrielles (osmose inverse).
- Le moteur du phénomène est la pression osmotique, créée par une différence de concentration entre deux milieux.
- On note que le type de soluté n’a pas d’importance, la pression osmotique totale d’un milieu dépend de la quantité totale de particules dissoutes, pas de leur nature.
Voici un schéma pour mieux comprendre le phénomène :
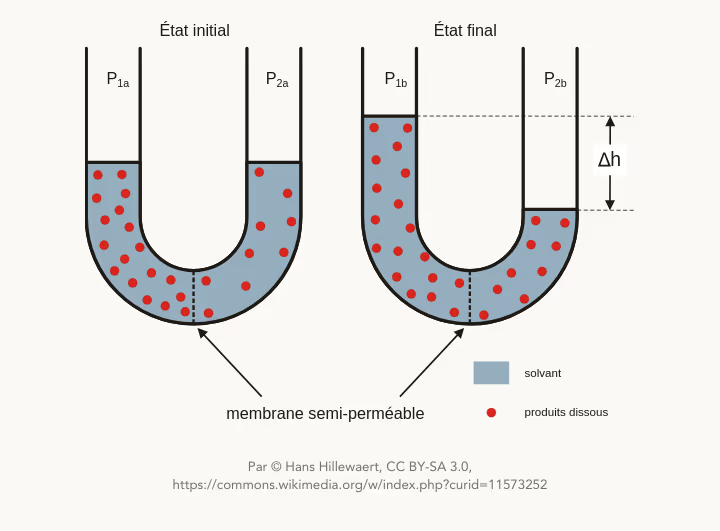
2. Mécanisme de l’osmose
2.1. Le rôle de la membrane
Les cellules des plantes et des animaux sont entourées d’une membrane biologique. Cette membrane est semi-perméable, ce qui veut dire qu’elle est sélective sur ce qui passe :
- L’eau passe librement,
- Les ions (Na⁺, Cl⁻) ou le sucre passent difficilement ou pas du tout.
Cette barrière est ce qui rend l’osmose possible en cuisine.
On note que lorsque l’on chauffe un ingrédient, cela va dégrader voir détruire cette membrane, c’est pour cela qu’une tomate qui chauffe va perdre son eau de végétation (attention ce n’est plus de l’osmose dans ce cas …).
2.2. Comment l’eau se déplace
Lorsqu’une différence de concentration apparaît :
- Si l’extérieur est plus salé / sucré, l’eau sort de la cellule pour diluer le milieu externe.
➜ La cellule se contracte, l’aliment s’assèche, se raffermit. - Si l’extérieur est moins concentré, l’eau entre dans la cellule.
➜ L’aliment gonfle, s’hydrate, se ramollit.
2.3. Effets typiques en cuisine
- Perte d’eau → texture plus ferme (saumon gravlax, légumes dégorgés…)
- Concentration des arômes internes
- Entrée de sel ou de sucre, mais uniquement après que l’eau est sortie
(la diffusion prend ensuite le relais).
2.4. Expérience illustrative amusante
Vous pouvez réaliser cette expérience à la maison avec un œuf et quelques produits basiques (eau, vinaigre blanc, sel ou sucre).
- Dans un récipient, mettre l’œuf entier (avec sa coquille) dans du vinaigre blanc :
- La réaction entre l’acide acétique du vinaigre et le carbonate de calcium de la coquille va produire du gaz carbonique et former des bulles en surface.
- Le calcium va se diluer progressivement dans l’eau jusqu’à ce que la coquille disparaisse complètement au bout de quelques heures.
- Quand la coquille a disparu, on ajoute beaucoup de sel ou de sucre dans le vinaigre :
- Cela va générer un décalage de pression osmotique entre l’œuf contenu à l’intérieur de sa membrane et le vinaigre contenant sel/sucre.
- Au bout de quelques minutes l’œuf va rétrécir et se ratatiner à cause de l’eau qui sort à cause du phénomène d’osmose.
- Retirons maintenant un peu de liquide et ajoutons de l’eau pure :
- Cela va à nouveau générer un décalage de pression osmotique mais cette fois-ci à l’avantage de l’œuf.
- Au bout de quelques minutes, notre œuf va se regonfler en absorbant de l’eau.
L’eau à donc migrer par osmose à travers la membrane de l’œuf ce qui se produit également avec les cellules de animaux et végétaux !
3. Applications culinaires
3.1. Le salage
Lorsque tu sales une viande ou un légume :
- Le sel à la surface crée un milieu dit « hypertonique » (très concentré).
- L’eau sort des cellules → dégorgement partiel via le phénomène d’osmose
- Le sel se dissout dans cette eau sortie.
- Cette saumure superficielle pénètre progressivement dans l’aliment (via le phénomène de diffusion).
Exemple : saumon gravlax
- En 1–2 h : perte d’eau importante → texture plus dense.
- En 12–24 h : pénétration progressive du sel → salaison homogène.
3.2. Le dégorgement (légumes, fruits)
Même logique, mais appliquée aux végétaux :
- Le sel attire l’eau hors des cellules.
- Les légumes se ramollissent légèrement et perdent de l’eau de végétation (amertume, humidité).
- Cela améliore ensuite la cuisson (moins d’eau rendue à la poêle, meilleure coloration).
Exemples : concombres, aubergines, courgettes.
3.3. Les marinades
Une marinade salée ou sucrée combine :
- Phénomène d’Osmose (sortie d’eau),
- Phénomène de Diffusion (entrée des arômes, du sel, des acides).
Points importants :
- Une marinade peu salée hydrate → texture plus tendre.
- Une marinade fortement salée déshydrate → texture ferme.
- Les acides (citron, vinaigre) n’agissent pas par osmose, mais modifient la perméabilité des membranes.
Exemple : poulet dans une saumure
→ léger salage + hydratation interne → jutosité accrue à la cuisson.
3.4. Le confisage au sucre
Le sucre agit comme le sel : milieu très concentré → sortie d’eau → pénétration lente du sucre.
Exemple : fruits confits
- Étape 1 : perte d’eau (phénomène osmotique).
- Étape 2 : remplacement progressif par le sucre (phénomène de diffusion lente).
- Résultat : texture dense, conservation longue.
3.5. Osmose et cuisson : interactions
À la cuisson :
- La chaleur fragilise les membranes → l’osmose devient moins sélective.
- Beaucoup d’eau sort (ex : viande saisie).
- Le salage préalable :
- Réduit la perte d’eau si fait à l’avance (salage à cœur)
- Augmente la perte d’eau si fait juste avant cuisson (sel attire l’eau à la surface).
Exemple : viande salée 40 min avant cuisson
→ meilleure rétention de jus.
4. Points de vigilance
👉 Bien doser le sel :
Un excès crée une déshydratation massive → texture trop ferme, goût trop salé.
👉 Tenir compte du temps :
L’osmose agit lentement, un salage express (juste avant la cuisson) ne produira pas un salage à cœur. On préconise de le faire au moins 1h avant la cuisson, si possible 24h avant pour une bonne pénétration du produit.
👉 Surveiller la température :
La chaleur détruit les membranes → l’osmose n’agit plus réellement, seule la diffusion domine.
👉 Attention aux légumes fragiles :
Le dégorgement peut trop ramollir certains légumes (ex : tomates).
👉 Sucre = Forte Osmose :
Le confisage est puissant → risque de texture “cuir” si trop rapide.
5. Lien entre Osmose, Diffusion et Activité de l’eau (Aw)
Les trois concepts sont intimement liés :
- Osmose : Mouvement de l’eau à travers une membrane semi-perméable (par ex. membranes cellulaires) mais sans mouvement des solutés.
- Diffusion : Mouvement spontané des solutés (ex : sel, sucres, arômes) vers des zones les plus concentrés vers les zones les moins concentrées.
- Activité de l’eau (Aw) : Part de l’eau du milieu/aliment pouvant se déplacer librement.
Leur combinaison permet de comprendre de nombreuses actions en cuisine : le confisage, la charcuterie, les textures de légume, le contrôle microbiologique, les saumures …
Exemple – Salage d’une tranche de concombre :
- Le sel abaisse l’Aw en surface.
- L’eau interne du légume migre vers l’extérieur du concombre par le phénomène d’osmose, ce qui fait dégorger le concombre (rendre son eau de végétation). Cela permet également de diluer une partie du sel dans cette eau de végétation.
- Cela conduit alors les molécules de sel à pénétrer et donc saler le concombre par le phénomène de diffusion.
- L’eau restante devient plus “attachée” aux solutés → Aw interne diminue.
- Résultat :
- Légume assoupli (car ayant dégorgé)
- Parfum concentré (car moins d’eau dans le concombre donc arôme moins dilués et plus de sel)
- Barrière antimicrobienne (car Aw inférieur et présence de sel)
Conclusion
L’osmose est un phénomène central en cuisine, intimement lié à la structure cellulaire des aliments. Elle explique la perte d’eau, la fermeté, la pénétration ultérieure du sel ou du sucre, et conditionne nombre de techniques traditionnelles : salage, dégorgement, marinades, confisage. Bien comprise, elle permet de contrôler texture, saveur, jutosité et même conservation.
Associée à la diffusion et à l’activité de l’eau, elle forme un trio fondamental pour comprendre la transformation culinaire. On vous recommande donc la lecture de ces deux articles pour clarifier l’ensemble des phénomènes que nous avons pu voir ici :
👉 Article sur la Diffusion
👉 Article sur l’Activité de l’Eau
Laisser un commentaire